印度加强医疗器械的监督
由Gunjan Bagla,Amritt,Inc。
 印度中央药物标准控制组织(CDSCO)是该国药物和医疗器械的国家监管机构(即,印度相当于美国的FDA)是在其内部提交的报告上行动药物技术咨询委员会(DTAB)在CDSCO下形成新部门。
印度中央药物标准控制组织(CDSCO)是该国药物和医疗器械的国家监管机构(即,印度相当于美国的FDA)是在其内部提交的报告上行动药物技术咨询委员会(DTAB)在CDSCO下形成新部门。
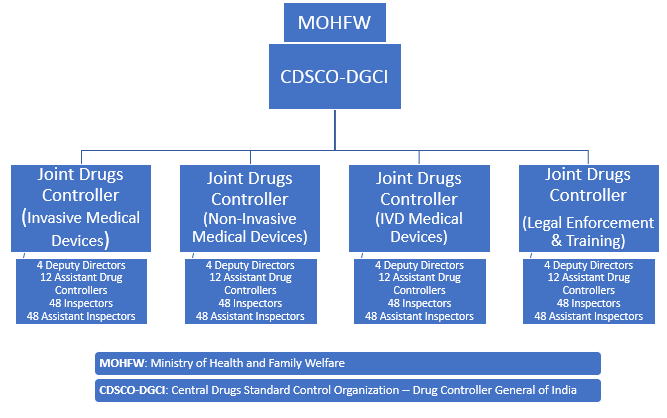
根据DTAB的提案 - 该国对药品和医疗器械相关技术事项的最高法定决策机构 - 新司及其军官将专门与医疗设备一起工作。冠状动脉支架,起搏器,矫形膝盖和臀部植入物,结构心脏装置,外围装置,内窥镜和体外诊断装置等重大关键护理装置预计将优先考虑。
图1 - 新部门的结构,如dtab所提出的
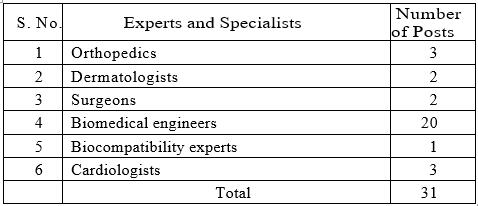
印度希望雇用治疗段的医生和外科医生涵盖骨科,皮肤病学,手术,生物医学工程,医学成像,心脏病学和生物相容性,以命名几个。此外,将建立五个实验室以测试设备和体外诊断。他们的位置尚未披露。
超过700人的人员,包括管理员和主题专家,将随着时间的推移被聘用新分部。鉴于监管机构需要进行简化规定,监测印度医疗器械的疗效和质量,并加强这一垂直的垂直,鉴于该数量,确定该号码。
700名拟议工作人员中有400人预计监督监管任务,例如制造地点的审计,进口批准,取消和许可证的批准等职责。剩余的新员工将在国家实验室中取出,以测试制造商在提交期间提出的医疗器械的安全性和有效性。
表1 - DCGI下CDSCO中的医疗设备垂直垂直

人员总数= 754
除了上述人员外,DTAB还提议在合同基础上招募一些专家,如下类别:
期望是CDSCO的人才搜索将主要集中在国内候选人身上。然而,由于美国签证问题,更多的印度外籍人士正在返回印度,其中一些人可能会发现这些机会有趣。政府将被这些培训的候选人所吸引。
行业专家觉得这部新部门的全面基础设施可能需要五年多的时间来创造和维持。CDSCO的当前资源强度甚至没有一半的数字。
销售进入印度的外国公司普遍欢迎锐利的专注于医疗器械与毒品不同,因为印度的预先存在的“抓住”规定未能适当调节许多设备课程。印度和一些中国公司已经与可能或可能不安全有效的产品跳进过这个无效,但大多数西方制造商更愿意在营销任何产品之前,在政府中批准。
这导致了一些西方公司避免了一些进入某些类别。他们的希望是,增加的监管和检查将震撼不总是遵循ISO 13485,六西格玛质量和良好制造业等国际标准的边际运营商。
编辑注意:在本文出版之前不久,印度宣布了一个出乎意料而深削减公司税率 - 在经济的当前规模上达到约200亿美元。结合所描述的监管变化,这一举措有可能严重影响国家的当前和未来的Medtech运营商。
政府削减了公司税率对于印度公司以22%的税率为22%,有效税率降至24.9%以前的34.9%(包括附加费和CESS),并将最低替代税率从18.5%降至15%。政府还宣布了2019年10月1日或之后的新公司的特价17%,并在2023年3月之前启动了新的制造工厂。
到了星期一(2019年3月23日)晚上,“SenseX”(类似于道琼斯平均水平)在3000点上升,总体股票价值占8%,标志着印度股市最佳的为期两天的性能见过。
金融部长NIRMALA SITHARAMAN在星期日(9/22/2019)表示,印度被拒绝作为投资目的地的首要考虑表现在比其他人都更好......对于那些正在推出新投资的人,没有国家提供15个国家分(基本税率,有效17%)。我们赋予15%,没有垫(最小替代税)和更简单的税收结构。“
您可以在税收变动找到作者的原始文章这里。
关于作者
Gunjan Bagla是董事总经理Amritt Inc.,一家加利福尼亚州的咨询公司专注于帮助美国公司在印度取得成功。他的客户包括Covidien(现在正在塞进塞尔彻西),Roche Diagnostics,BD,Lifenet Health,Johnson&Johnson,Gojo等。他在纽约时报,洛杉矶时报,以及华盛顿邮政以及彭博电视台,BBC电视台和福克斯商业新闻。他还为哈佛商业评论写了关于印度。Gunjan拥有南伊利诺伊州南部大学的MBA,是印度印度理工学院(IIT)Kanpur的机械工程学位。
资源
http://www.theiniadexpert.com/india-to-streamline-regulatory-overight-of-medical-device.

